Nat Med | Հաստ աղիքի քաղցկեղի ինտեգրված ուռուցքային, իմունային և մանրէային լանդշաֆտի քարտեզագրման բազմաօմիկ մոտեցումը բացահայտում է միկրոբիոմի փոխազդեցությունը իմունային համակարգի հետ
Չնայած վերջին տարիներին առաջնային հաստ աղիքի քաղցկեղի բիոմարկերները լայնորեն ուսումնասիրվել են, ներկայիս կլինիկական ուղեցույցները բուժման առաջարկությունները որոշելու համար հիմնվում են միայն ուռուցք-ավշային հանգույց-մետաստազների փուլավորման և ԴՆԹ-ի անհամապատասխանության վերականգնման (MMR) արատների կամ միկրոսատելիտային անկայունության (MSI) հայտնաբերման վրա (բացի ստանդարտ պաթոլոգիական թեստավորումից): Հետազոտողները նկատել են գեների արտահայտման վրա հիմնված իմունային պատասխանների, մանրէային պրոֆիլների և ուռուցքի ստրոմայի միջև կապի բացակայություն քաղցկեղի գենոմի ատլասի (TCGA) հաստ աղիքի քաղցկեղի կոհորտում և հիվանդների գոյատևման միջև:
Հետազոտությունների զարգացմանը զուգընթաց, հայտնաբերվել է, որ առաջնային հաստ աղիքի քաղցկեղի քանակական բնութագրերը, ներառյալ քաղցկեղի բջջային, իմունային, ստրոմալ կամ մանրէային բնույթը, զգալիորեն կապված են կլինիկական արդյունքների հետ, սակայն դեռևս սահմանափակ է պատկերացում այն մասին, թե ինչպես են դրանց փոխազդեցությունները ազդում հիվանդների արդյունքների վրա։
Ֆենոտիպային բարդության և արդյունքի միջև կապը վերլուծելու համար Կատարի Սիդրա բժշկական հետազոտությունների ինստիտուտի հետազոտողների թիմը վերջերս մշակել և վավերացրել է ինտեգրված միավոր (mICRoScore), որը նույնականացնում է լավ գոյատևման մակարդակ ունեցող հիվանդների խումբը՝ համատեղելով միկրոբիոմի բնութագրերը և իմունային մերժման հաստատունները (ICR): Թիմը կատարել է առաջնային հաստ աղիքի քաղցկեղով 348 հիվանդներից վերցված թարմ սառեցված նմուշների համապարփակ գենոմիկ վերլուծություն, ներառյալ ուռուցքների ՌՆԹ-ի հաջորդականացումը և համապատասխանեցված առողջ հաստ աղիքի հյուսվածքը, ամբողջ էկզոմի հաջորդականացումը, խորը T-բջջային ընկալիչի և 16S բակտերիալ rRNA գեների հաջորդականացումը, լրացված ամբողջ ուռուցքի գենոմի հաջորդականացմամբ՝ միկրոբիոմը ավելի մանրամասն բնութագրելու համար: Ուսումնասիրությունը հրապարակվել է Nature Medicine-ում՝ որպես «Հաստ աղիքի քաղցկեղի ինտեգրված ուռուցքային, իմունային և միկրոբիոմային ատլաս»:

Հոդվածը հրապարակվել է Nature Medicine-ում
AC-ICAM-ի ակնարկ
Հետազոտողները օգտագործել են օրթոգոնալ գենոմիկ հարթակ՝ թարմ սառեցված ուռուցքի նմուշները վերլուծելու և հարակից առողջ հաստ աղիքի հյուսվածքը (ուռուցք-նորմալ զույգեր) համապատասխանեցնելու համար այն հիվանդներից, որոնց մոտ հաստ աղիքի քաղցկեղի հյուսվածաբանական ախտորոշում էր եղել առանց համակարգային թերապիայի: Ամբողջ էկզոմի հաջորդականության (WES), RNA-seq տվյալների որակի վերահսկողության և ներառման չափանիշների սկրինինգի հիման վրա, 348 հիվանդներից վերցված գենոմիկ տվյալները պահպանվել և օգտագործվել են հետագա վերլուծության համար՝ 4.6 տարի միջին հետազոտական ժամանակահատվածով: Հետազոտական խումբն այս ռեսուրսն անվանել է Sidra-LUMC AC-ICAM: Իմուն-քաղցկեղ-միկրոբիոմի փոխազդեցությունների քարտեզ և ուղեցույց (Նկար 1):
Մոլեկուլային դասակարգում՝ օգտագործելով ICR
Իմունային գենետիկական մարկերների մոդուլային հավաքածու գրանցելով քաղցկեղի շարունակական իմունային հսկողության համար, որը կոչվում է մերժման իմունային հաստատուն (ՄՄՀ), հետազոտական խումբը օպտիմալացրել է ՄՄՀ-ն՝ այն խտացնելով 20 գեներից բաղկացած վահանակի մեջ, որը ներառում է քաղցկեղի տարբեր տեսակներ, այդ թվում՝ մելանոման, միզապարկի քաղցկեղը և կրծքագեղձի քաղցկեղը: ՄՄՀ-ն նաև կապված է իմունաթերապիայի արձագանքի հետ քաղցկեղի տարբեր տեսակների, այդ թվում՝ կրծքագեղձի քաղցկեղի դեպքում:
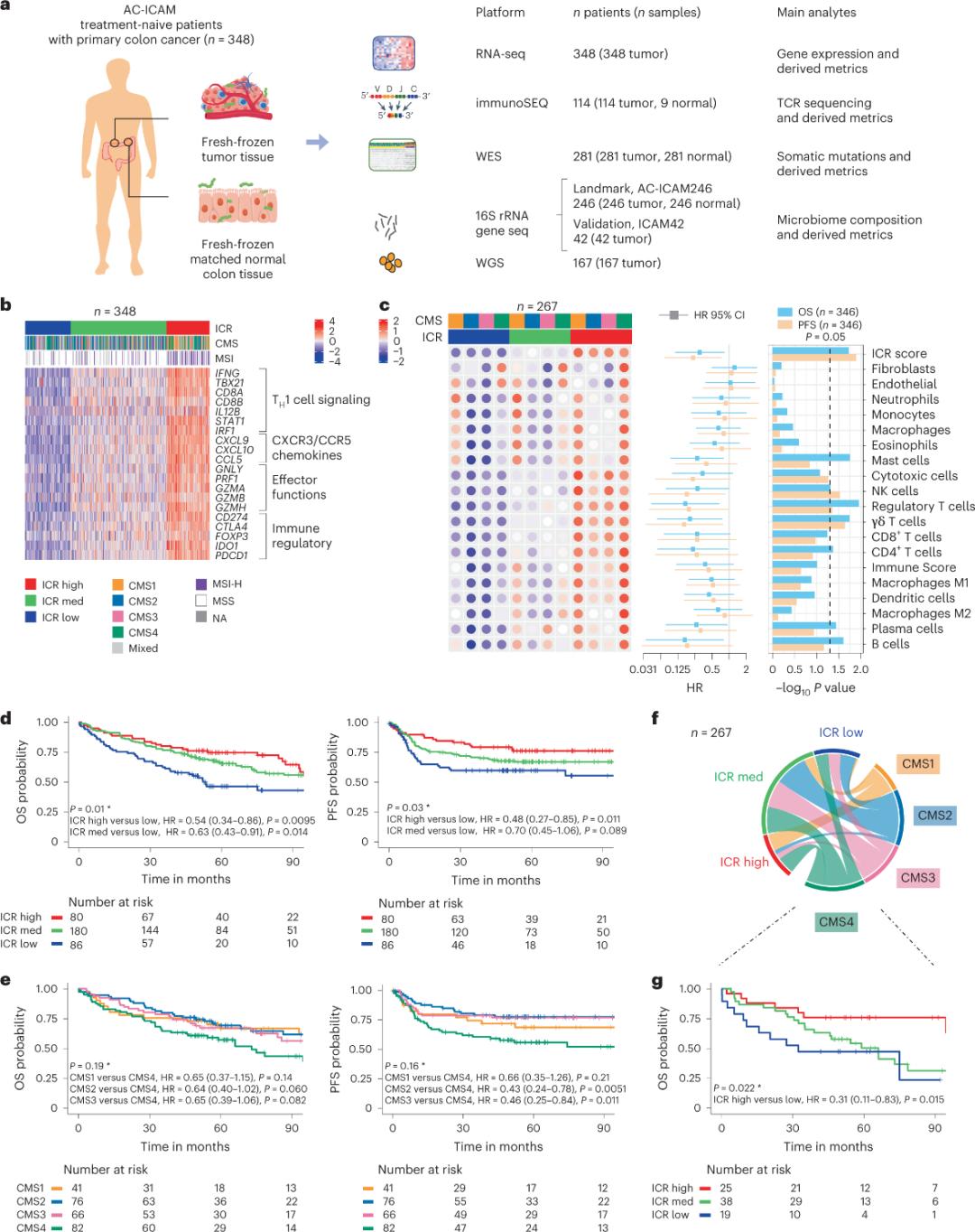
Նախ, հետազոտողները վավերացրին AC-ICAM կոհորտի ICR ստորագրությունը՝ օգտագործելով ICR գեների վրա հիմնված համատեղ դասակարգման մոտեցում՝ կոհորտը դասակարգելու երեք կլաստերների/իմունային ենթատիպերի՝ բարձր ICR (տաք ուռուցքներ), միջին ICR և ցածր ICR (սառը ուռուցքներ) (Նկար 1բ): Հետազոտողները բնութագրել են կոնսենսուսային մոլեկուլային ենթատիպերի (CMS) հետ կապված իմունային հակումը, որը հաստ աղիքի քաղցկեղի տրանսկրիպտոմների վրա հիմնված դասակարգում է: CMS կատեգորիաները ներառում էին CMS1/իմուն, CMS2/կանոնիկ, CMS3/մետաբոլիկ և CMS4/մեզենքիմալ: Վերլուծությունը ցույց տվեց, որ ICR միավորները բացասականորեն կապված էին քաղցկեղի որոշակի բջջային ուղիների հետ CMS բոլոր ենթատիպերում, և իմունոսուպրեսիվ և ստրոմալ-կապված ուղիների հետ դրական կապեր նկատվել են միայն CMS4 ուռուցքների մոտ:
Բոլոր CMS-ներում բնական մարդասպան (NK) բջիջների և T բջիջների ենթաբազմությունների առատությունը ամենաբարձրն էր ICR բարձր իմունային մակարդակ ունեցող ենթատիպերում, իսկ լեյկոցիտների այլ ենթաբազմություններում՝ ավելի մեծ փոփոխականությամբ (Նկար 1գ): ICR իմունային ենթատիպերն ունեին տարբեր գոյատևում և առաջընթաց կյանք՝ ICR-ի աստիճանական աճով՝ ցածրից բարձր (Նկար 1դ), ինչը հաստատում է ICR-ի կանխատեսողական դերը հաստ աղիքի քաղցկեղի դեպքում:
Նկար 1. AC-ICAM ուսումնասիրության դիզայնը, իմունային համակարգի հետ կապված գեների ստորագրությունը, իմունային և մոլեկուլային ենթատիպերը և գոյատևումը։
ICR-ը որսում է ուռուցքով հարստացված, կլոնալ ուժեղացված T բջիջները
Ուռուցքային հյուսվածք ներթափանցող T բջիջների միայն փոքր մասն է սպեցիֆիկ ուռուցքային հակածինների համար (10%-ից պակաս): Հետևաբար, ուռուցքի ներսում T բջիջների մեծ մասը կոչվում է կողմնակի T բջիջներ (կողքից T բջիջներ): Առավելագույնս ուժեղ կապը արտադրողական TCR-ներով ավանդական T բջիջների քանակի հետ դիտվել է ստրոմալ բջիջների և լեյկոցիտների ենթապոպուլյացիաներում (հայտնաբերվել են RNA-seq-ի միջոցով), որոնք կարող են օգտագործվել T բջիջների ենթապոպուլյացիաները գնահատելու համար (Նկար 2ա): ICR կլաստերներում (ընդհանուր և CMS դասակարգում) իմունային SEQ TCR-ների ամենաբարձր կլոնայինությունը դիտվել է ICR-բարձր և CMS ենթատիպ CMS1/իմուն խմբերում (Նկար 2գ), որտեղ ICR-բարձր ուռուցքների ամենաբարձր համամասնությունն է եղել: Օգտագործելով ամբողջ տրանսկրիպտոմը (18,270 գեն), վեց ICR գեներ (IFNG, STAT1, IRF1, CCL5, GZMA և CXCL10) TCR իմունային SEQ կլոնայինության հետ դրականորեն կապված տասը լավագույն գեների շարքում էին (Նկար 2դ): ImmunoSEQ TCR կլոնականությունն ավելի ուժեղ է համընկնում ICR գեների մեծ մասի հետ, քան ուռուցքի նկատմամբ զգայուն CD8+ մարկերների միջոցով դիտարկված համընկումները (Նկար 2f և 2g): Եզրափակելով՝ վերը նշված վերլուծությունը ենթադրում է, որ ICR ստորագրությունը արտացոլում է ուռուցքով հարստացված, կլոնային ուժեղացված T բջիջների առկայությունը և կարող է բացատրել դրա կանխատեսողական նշանակությունը:
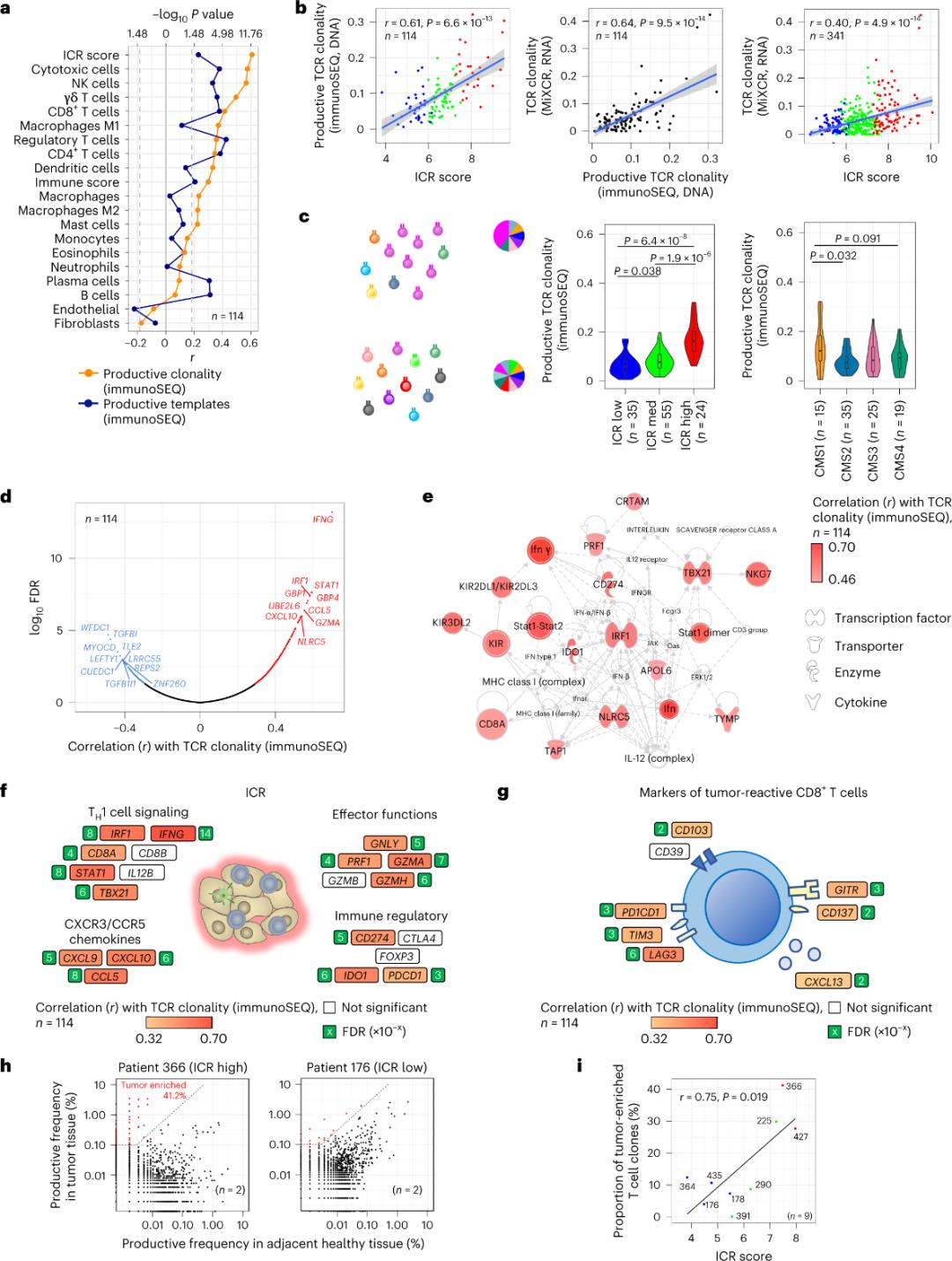
Նկար 2. TCR չափանիշներ և իմունային համակարգի հետ կապված գեների, իմունային և մոլեկուլային ենթատիպերի հետ փոխհարաբերությունը։
Միկրոբիոմի կազմը առողջ և հաստ աղիքի քաղցկեղի հյուսվածքներում
Հետազոտողները կատարել են 16S rRNA հաջորդականության որոշում՝ օգտագործելով 246 հիվանդի համապատասխան ուռուցքից և առողջ հաստ աղիքի հյուսվածքից արդյունահանված ԴՆԹ-ն (Նկար 3ա): Հաստատման համար հետազոտողները լրացուցիչ վերլուծել են 16S rRNA գեների հաջորդականության որոշումը լրացուցիչ 42 ուռուցքի նմուշներից, որոնք չունեին վերլուծության համար հասանելի համապատասխան նորմալ ԴՆԹ: Նախ, հետազոտողները համեմատել են համապատասխան ուռուցքների և առողջ հաստ աղիքի հյուսվածքի միջև բուսական աշխարհի հարաբերական առատությունը: Clostridium perfringens-ը զգալիորեն աճել էր ուռուցքներում՝ համեմատած առողջ նմուշների հետ (Նկար 3ա-3դ): Ալֆա բազմազանության (տեսակների բազմազանություն և առատություն մեկ նմուշում) մեջ նշանակալի տարբերություն չի եղել ուռուցքի և առողջ նմուշների միջև, և միկրոբային բազմազանության չնչին նվազում է նկատվել ICR-բարձր ուռուցքների մոտ՝ համեմատած ICR-ցածր ուռուցքների հետ:
Մանրէային պրոֆիլների և կլինիկական արդյունքների միջև կլինիկորեն նշանակալի կապերը հայտնաբերելու համար հետազոտողները նպատակ ունեին օգտագործել 16S rRNA գեների հաջորդականության տվյալները՝ միկրոբիոմի գոյատևումը կանխատեսող առանձնահատկությունները բացահայտելու համար: AC-ICAM246-ում հետազոտողները կիրառել են OS Cox ռեգրեսիոն մոդել, որն ընտրել է 41 առանձնահատկություն՝ ոչ զրոյական գործակիցներով (կապված դիֆերենցիալ մահացության ռիսկի հետ), որոնք կոչվում են MBR դասակարգիչներ (Նկար 3f):
Այս ուսումնական խմբում (ICAM246) ցածր MBR միավորը (MBR<0, ցածր MBR) կապված էր մահվան զգալիորեն ցածր ռիսկի հետ (85%): Հետազոտողները հաստատել են ցածր MBR-ի (ռիսկի) և երկարատև գոյատևման միջև կապը երկու անկախ վավերացված խմբերում (ICAM42 և TCGA-COAD): (Նկար 3) Ուսումնասիրությունը ցույց է տվել ուժեղ կապ էնդոգաստրիկ կոկերի և MBR միավորների միջև, որոնք նման էին ուռուցքային և առողջ հաստ աղիքի հյուսվածքներում:
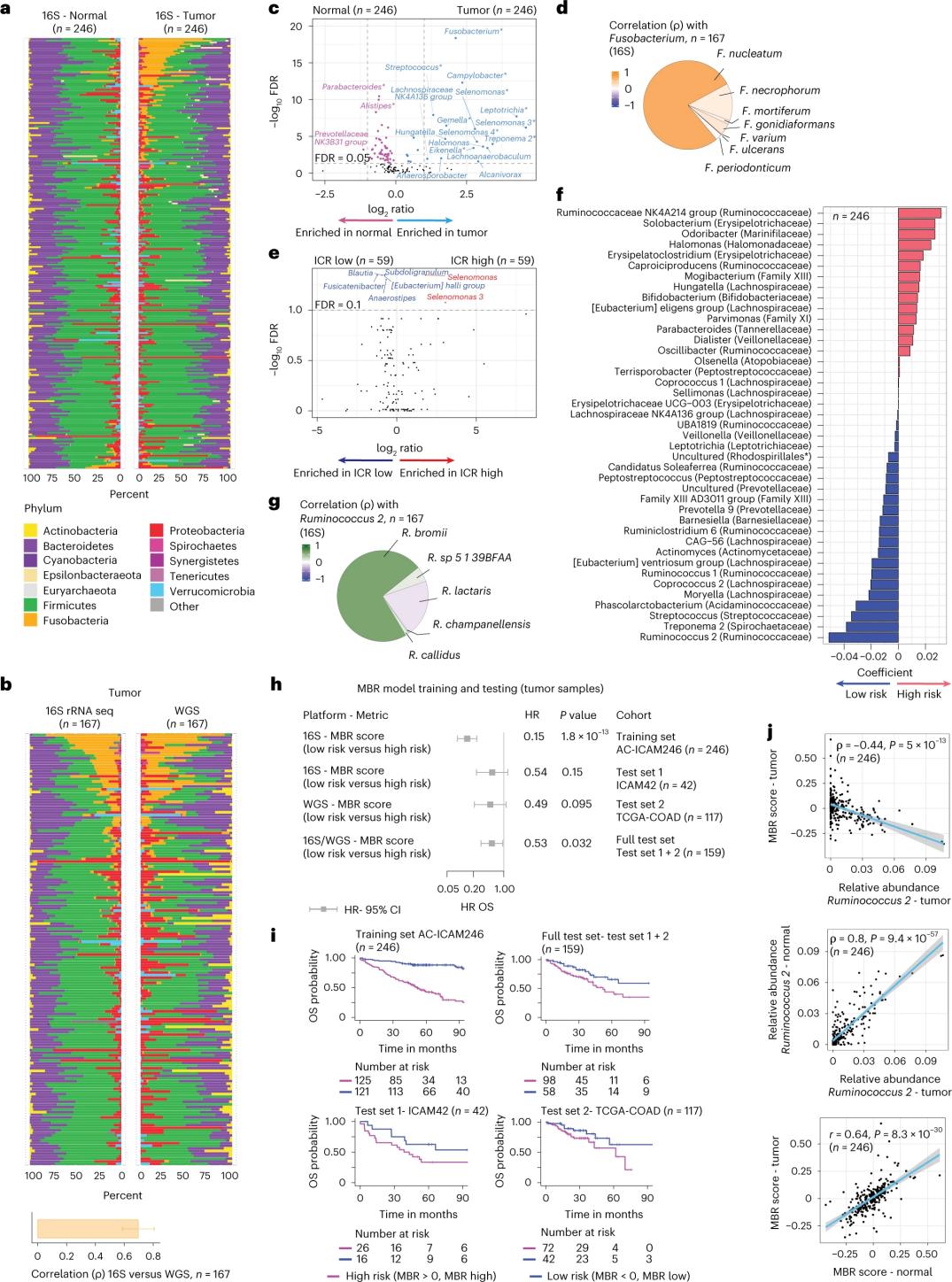
Նկար 3. Ուռուցքի և առողջ հյուսվածքների միկրոբիոմը և դրա կապը ICR-ի և հիվանդների գոյատևման հետ։
Եզրակացություն
Այս ուսումնասիրության մեջ օգտագործված բազմաօմիկ մոտեցումը հնարավորություն է տալիս մանրակրկիտ հայտնաբերել և վերլուծել հաստ աղիքի քաղցկեղի իմունային պատասխանի մոլեկուլային ստորագրությունը և բացահայտում է միկրոբիոմի և իմունային համակարգի միջև փոխազդեցությունը: Ուռուցքի և առողջ հյուսվածքների խորը TCR հաջորդականացումը ցույց տվեց, որ ICR-ի կանխատեսողական ազդեցությունը կարող է պայմանավորված լինել ուռուցքով հարստացված և հնարավոր է՝ ուռուցքի հակածին-սպեցիֆիկ T բջջային կլոնները որսալու դրա ունակությամբ:
AC-ICAM նմուշներում 16S rRNA գեների հաջորդականության միջոցով ուռուցքի միկրոբիոմի կազմը վերլուծելով՝ թիմը նույնականացրեց միկրոբիոմի ստորագրություն (MBR ռիսկի գնահատական)՝ ուժեղ կանխատեսողական արժեքով: Չնայած այս ստորագրությունը ստացվել էր ուռուցքի նմուշներից, առողջ հաստ աղիքի և ուռուցքի MBR ռիսկի գնահատականի միջև կար ուժեղ կապ, ինչը ենթադրում է, որ այս ստորագրությունը կարող է արտացոլել հիվանդների աղիքային միկրոբիոմի կազմը: ICR և MBR գնահատականները համատեղելով՝ հնարավոր եղավ նույնականացնել և վավերացնել բազմամակարդակ ուսանողական բիոմարկեր, որը կանխատեսում է հաստ աղիքի քաղցկեղով հիվանդների գոյատևումը: Ուսումնասիրության բազմամակարդակ տվյալների բազան հնարավորություն է տալիս ավելի լավ հասկանալ հաստ աղիքի քաղցկեղի կենսաբանությունը և օգնել բացահայտել անհատականացված թերապևտիկ մոտեցումներ:
Հրապարակման ժամանակը. Հունիս-15-2023
 中文网站
中文网站